Помимо технологий, синтез гликозидов всегда представлял интерес для науки, поскольку это очень распространённая реакция в природе. Недавние статьи Шмидта, Тошимы и Тацуты, а также многочисленные цитируемые в них источники, демонстрируют широкий спектр синтетических возможностей.
В синтезе гликозидов многосахарные компоненты комбинируются с нуклеофилами, такими как спирты, углеводы или белки. Если требуется селективная реакция с одной из гидроксильных групп углевода, все остальные функции должны быть защищены на первом этапе. В принципе, ферментативные или микробные процессы, благодаря своей селективности, могут заменить сложные этапы химической защиты и снятия защиты для селективного выделения гликозидов из отдельных участков. Однако, ввиду долгой истории алкилгликозидов, применение ферментов в синтезе гликозидов не получило широкого изучения и применения.
Из-за мощности соответствующих ферментных систем и высоких затрат на производство ферментативный синтез алкилполигликозидов пока не готов к выводу на промышленный уровень, и предпочтение отдается химическим методам.
В 1870 году Макколи сообщил о синтезе «ацетохлоргидрозы» (1, рисунок 2) путем реакции декстрозы (глюкозы) с ацетилхлоридом, что в конечном итоге привело к истории путей синтеза гликозидов.
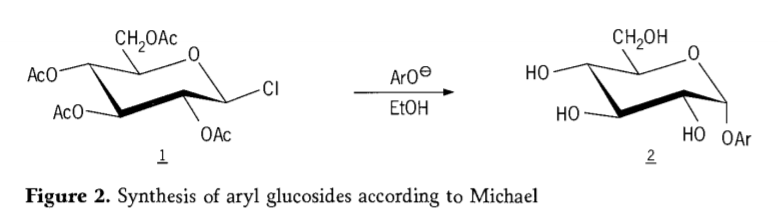
Тетра-0-ацетилглюкопиранозилгалогениды (ацетогалогенглюкозы) впоследствии оказались полезными промежуточными продуктами для стереоселективного синтеза чистых алкилглюкозидов. В 1879 году Артуру Майклу удалось получить определённые кристаллизующиеся арилгликозиды из промежуточных продуктов Колли и фенолятов (Aro-, рис. 2).
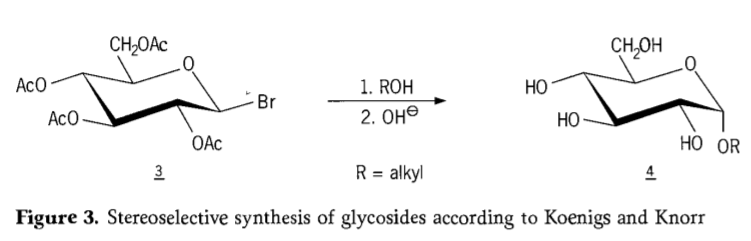
В 1901 году Михаэль предложил синтез широкого спектра углеводов и гидроксильных агликонов, когда В. Кёнигс и Э. Кнорр представили усовершенствованный стереоселективный процесс гликозидирования (рис. 3). Реакция включает SN2-замещение у аномерного атома углерода и протекает стереоселективно с инверсией конфигурации, образуя, например, α-глюкозид 4 из β-аномера промежуточного продукта ацеобромглюкозы 3. Синтез Кёнигса-Кнорра протекает в присутствии серебряных или ртутных промоторов.
В 1893 году Эмиль Фишер предложил принципиально иной подход к синтезу алкилглюкозидов. Этот процесс сейчас хорошо известен как «гликозидирование по Фишеру» и представляет собой кислотно-катализируемую реакцию гликозидов со спиртами. Тем не менее, любой исторический источник должен также включать в себя первую попытку А. Готье, предпринятую в 1874 году, преобразовать декстрозу безводным этанолом в присутствии соляной кислоты. Из-за ошибочного элементного анализа Готье решил, что получил «диглюкозу». Позже Фишер продемонстрировал, что «диглюкоза» Готье на самом деле представляла собой преимущественно этилглюкозид (рис. 4).
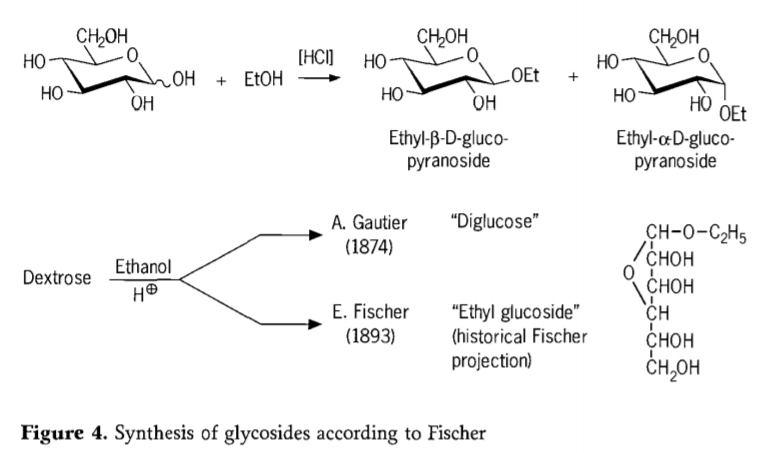
Фишер правильно определил структуру этилглюкозида, что видно из предложенной исторической фуранозидной формулы. Фактически, продукты гликозидирования по Фишеру представляют собой сложные, преимущественно равновесные смеси α/β-аномеров и изомеров пиранозида/фуранозида, которые также включают случайно связанные гликозидные олигомеры.
Соответственно, отдельные молекулярные частицы сложно выделить из реакционных смесей Фишера, что в прошлом представляло серьёзную проблему. После некоторого усовершенствования этого метода синтеза Фишер впоследствии применил синтез Кёнигса-Кнорра для своих исследований. Используя этот метод, Э. Фишер и Б. Хельферих в 1911 году впервые сообщили о синтезе длинноцепочечного алкилглюкозида, проявляющего свойства поверхностно-активного вещества.
Ещё в 1893 году Фишер справедливо отметил важные свойства алкилгликозидов, такие как их высокая устойчивость к окислению и гидролизу, особенно в сильнощелочных средах. Обе эти характеристики ценны для алкилполигликозидов, используемых в качестве поверхностно-активных веществ.
Исследования, связанные с реакцией гликозидирования, продолжаются, и в последнее время было разработано несколько интересных методов получения гликозидов. Некоторые процедуры синтеза гликозидов представлены на рисунке 5.
В целом процессы химического гликозидирования можно разделить на процессы, приводящие к сложным олигомерным равновесиям в кислотно-катализируемом гликозильном обмене.
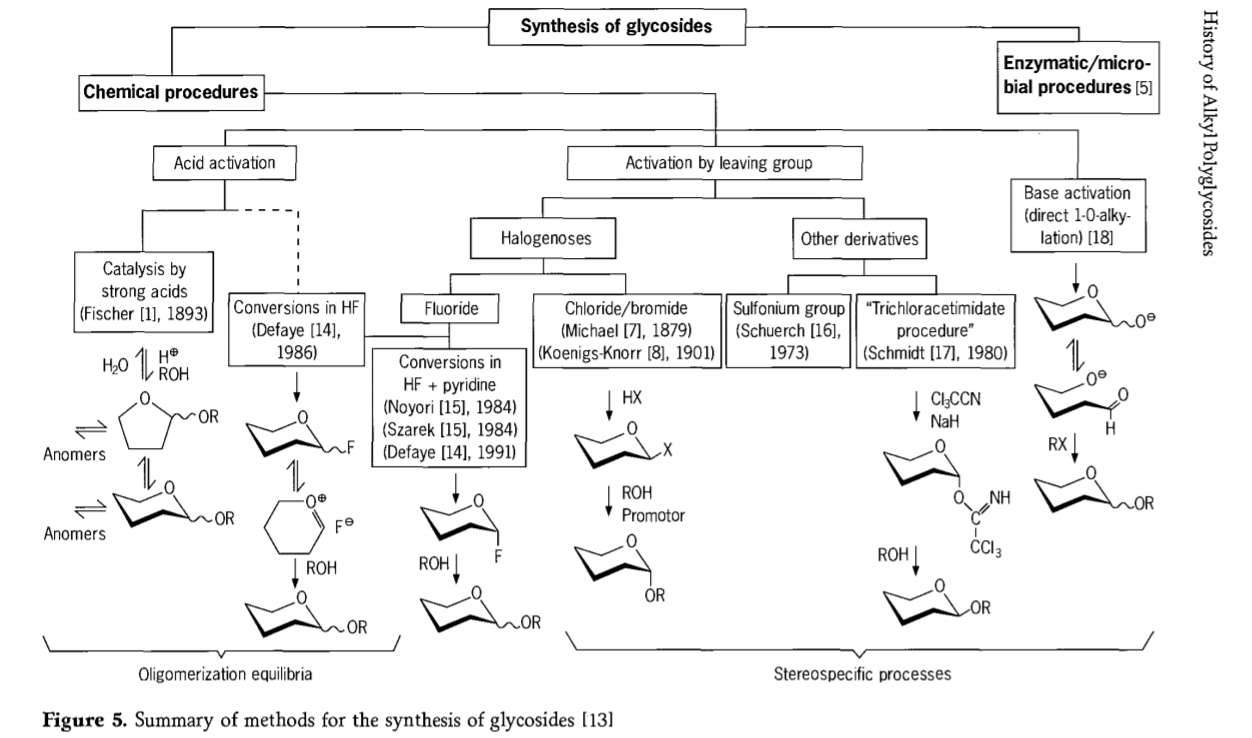
Реакции на соответствующим образом активированных углеводных субстратах (гликозидные реакции Фишера и реакции с фтористым водородом (HF) с незащищенными молекулами углеводов) и кинетически контролируемые, необратимые и преимущественно стереотаксические реакции замещения. Второй тип процедур может привести к образованию отдельных молекул, а не сложных смесей реакций, особенно в сочетании с методами консервативных групп. Углеводы могут оставлять группы на эктопическом атоме углерода, такие как атомы галогенов, сульфонильные или трихлорацетимидатные группы, или активироваться основаниями перед превращением в трифлатные эфиры.
В частном случае гликозидирования во фтористом водороде или в смесях фтористого водорода и пиридина (пиридиний полифторид) гликозилфториды образуются in situ и легко превращаются в гликозиды, например, со спиртами. Было показано, что фтористый водород является сильно активирующей, неразрушающей реакционной средой; наблюдается равновесная автоконденсация (олигомеризация), аналогичная реакции Фишера, хотя механизм реакции, вероятно, иной.
Химически чистые алкилгликозиды подходят только для очень специфических применений. Например, алкилгликозиды успешно использовались в биохимических исследованиях для кристаллизации мембранных белков, таких как трёхмерная кристаллизация порина и бактериородопсина в присутствии октил-β-D-глюкопиранозида (дальнейшие эксперименты, основанные на этой работе, привели к Нобелевской премии по химии, присуждённой Дайзенхоферу, Хуберу и Мишелю в 1988 году).
В ходе разработки алкилполигликозидов стереоселективные методы использовались в лабораторном масштабе для синтеза различных модельных веществ и изучения их физико-химических свойств. В связи со сложностью процесса, нестабильностью промежуточных соединений, а также количеством и критическим характером отходов, синтез по методу Кёнигса-Кнорра и другими методами с защитными группами создавал значительные технические и экономические проблемы. Процессы типа Фишера сравнительно менее сложны и проще в реализации в промышленных масштабах, поэтому они являются предпочтительным методом для производства алкилполигликозидов в больших масштабах.
Время публикации: 12 сентября 2020 г.





